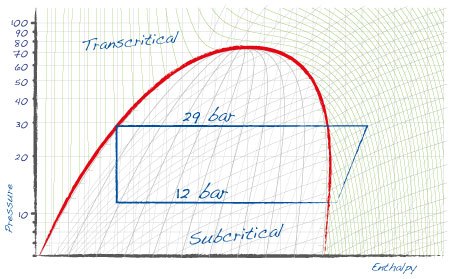
Diagrama de Mollier
El diagrama de Mollier es la tabla en la cual pueden representarse en un punto las condiciones del refrigerante en cualquier estado termodinámico y en cualquier parte del ciclo. A veces esta tabla se menciona como «tabla P-h» o «tabla presión-entalpía».
Dicho de otra forma, el diagrama Ph, o diagrama de Mollier para presión entalpía, es la representación gráfica en una carta semilogarítmica en el plano Presión/entalpía de los estados posibles de un compuesto químico —especialmente para los gases refrigerantes— y es en ella donde se trazan y suelen estudiar los distintos sistemas frigoríficos de refrigeración por compresión.
Básicamente el diagrama está compuesto por dos ejes principales y tres zonas delimitadas por una curva de saturación.
- En el eje de las ordenadas se registra el valor de Presión absoluta en (bar) -para diagramas Ph en SI-, eje graduado en escala logarítmica.
- En el eje de las abcisas se registra el valor de entalpía en unidad de masa en [kJ/kg] ó [kcal/kg].
- Una curva de saturación con forma de “U” invertida la cual determina si el compuesto se encuentra en estado de: líquido subenfriado, líquido saturado, mezcla líquido-vapor, vapor saturado o vapor sobrecalentado.
A su vez se definen seis tipos de trazas a través de las cuales se describen los ciclos de refrigeración y los estados de agregación de la materia.
- Isobaras: Rectas paralelas que coinciden iguales valores de presión. Estas son perpendiculares al eje de las ordenadas.
- Isoentálpicas: Rectas paralelas que coinciden iguales valores de entalpía en masa. Estas son perpendiculares al eje de las abcisas.
- Isotermas: que en la zona de líquido subenfriado son paralelas a la ordenada y dentro de la campana de mezcla son paralelas a la abcisa, y en la zona de vapor sobrecalentado descienden en forma curva. Estas trazas –“paralelas” entre sí- coinciden los valores de igual temperatura del sistema, y en las tablas Ph en el SI está expresado en grados Celsius.
- Isócoras: Son las curvas que coinciden los puntos con igual volumen específico y también son paralelas entre sí para distintos valores. En el SI está expresado en [m³/kg]. Se desarrollan en la izquierda de la zona de mezcla líquido-vapor y se extiende hacia la derecha hasta la de vapor sobrecalentado hasta el final del diagrama.
- Isoentrópicas: Son las curvas que coinciden los valores de igual entropía en el sistema. En el SI se miden en [kJ/kg K] ó [kJ/kg°C]. Paralelas entre sí y de una elevada pendiente.
- Nueve curvas de «título de vapor» o «calidad de vapor» que indican el porcentaje en masa de vapor contenido en la mezcla líquido-vapor. Estas curvas, existentes sólo dentro de la campana de mezcla, son coincidentes en su extremo superior mas su extremo inferior se encuentra relativamente equidistante a la adyacente y así sucesivamente. Son nominadas con los valores del 0,1 al 0,9.
En la parte superior de la curva de saturación se define el llamado punto crítico el cual es el límite a partir del que, por mucho que se aumente la presión, no es posible condensar el gas.
A continuación te explicamos con detalle toda la teoría para aprender este complejo diagrama que todo técnico en frío y calor debe conocer.
Puedes descargarte esta presentación en este enlace.
Se puede ampliar más información en este documento.
| Diagramas de Mollier, en PDF, de distintos refrigerantes | |||
| R13 | R32 | R134a | R404A |
| R407C | R410a | ||
| R449A | |||
| R1233zd(E) | R1234yf | R1234ze(E) | |
| R290 | R600a | ||
| R717 | R744 | ||